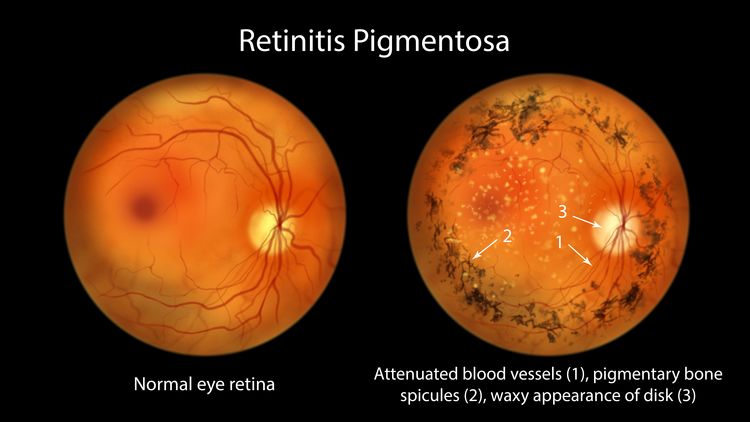
Die Augenerkrankung Retinitis pigmentosa lässt Sinneszellen der Netzhaut absterben und führt deshalb oft zur Erblindung. Oldenburger Forschende wollen jetzt herausfinden, wie der genetische Defekt eines bestimmten Gens, des RPGR-Gens, diese Krankheit verursacht.
Zuerst können sie in der Nacht nicht mehr gut sehen, später verengt sich auch tagsüber das Blickfeld: Menschen, die an Retinitis pigmentosa leiden, bemerken das oft im frühen Erwachsenenalter. Absterbende Netzhautzellen führen zu Einschränkungen beim Sehen, in vielen Fällen schließlich auch zur Erblindung. Denn heilbar ist die Krankheit in der Regel nicht. Einer von 4.000 Menschen ist von einer krankheitsassoziierten Genvariante betroffen, die zu Retinitis pigmentosa führt.
„Damit zählt sie zu den sogenannten seltenen Erkrankungen, ist unter diesen aber vergleichsweise häufig und schränkt die Lebensqualität für Betroffene massiv ein“, sagt Prof. Dr. John Neidhardt, Leiter der Abteilung Humangenetik am Department für Humanmedizin der Universitätsmedizin Oldenburg. Er forscht bereits seit vielen Jahren zu den Ursachen und Mechanismen dieser Krankheit. Jetzt fördern das Land Niedersachsen und die VolkswagenStiftung seine Arbeit im Rahmen des Programms „zukunft.niedersachsen“ als eines von neun niedersächsischen Forschungsprojekten zu seltenen Erkrankungen. Rund 700.000 Euro fließen in das Oldenburger Projekt „Pioneering towards novel RPGR functions and innovative therapeutic approaches”.
Ursache für die Krankheit ist immer ein Gendefekt. Mehr als 80 Gene können eine Retinitis pigmentosa potenziell auslösen. Eines von ihnen ist RPGR, ein Gen auf dem X-Chromosom, dessen Veränderung - meist bei jungen Männern - der Grund dafür ist, dass Photorezeptoren im Auge absterben. Betroffene können auch völlig erblinden. „Noch gibt es keine zugelassene und wirksame Behandlung. Ärztinnen und Ärzte können im Moment leider nicht viel tun, um die Krankheit zu behandeln oder deren Fortschreiten zu verlangsamen, geschweige denn, aufzuhalten.“, erklärt Neidhardt.
Eine große Hoffnung liegt auf gentherapeutischen Ansätzen, die es ermöglichen, das defekte Gen durch ein Gesundes zu ersetzen. Das ist jedoch bisher nicht gut genug gelungen. Gerade erst musste ein Biotechnologie-Unternehmen bekanntgeben, dass sich bei einer gentherapeutischen Patientenstudie keine eindeutigen Verbesserungen zeigten.
„Wir müssen noch besser verstehen, wie genau RPGR funktioniert“, sagt Neidhardt. Unter anderem darauf zielt das jetzt geförderte Projekt ab. Konkret will das Humangenetik-Team herausfinden, welche Funktionen die verschiedenen Varianten des Proteins haben, die in den Zellen auf Basis des RPGR-Bauplans entstehen.
Außerdem will Neidhardt durchschauen, wie der Prozess funktioniert, der von der Genveränderung über viele Zwischenschritte - in einer Art biologischen Schadenskette - zum Absterben der Sinneszellen in der Netzhaut führt. „Nur dann, wenn wir diese Pathomechanismen im Detail verstehen, können wir auf dieser Basis wirksame Therapieansätze erarbeiten.“, sagt Neidhardt. Denkbar wäre zum Beispiel, dass sich daraus Ansätze ergeben, mit denen sich die Schadenskette medikamentös unterbrechen lässt, ohne dass eine aufwändige und kostspielige Gentherapie notwendig ist.
„Unsere Arbeit liegt sozusagen zwischen Grundlagen- und translationaler Forschung: Wir schaffen mehr als nur ein Grundverständnis für Prozesse, sondern entwickeln Ideen für neue Therapieansätze. Bevor diese zu den Patienten gelangen, sind aber noch weitere forschungsintensive Zwischenschritte nötig“, betont der Leiter der Humangenetik an der Universität Oldenburg.